جدول تناوبی عناصر شیمیایی نمایشی از عناصر شیمیایی است که براساس ساختار الکترونی مرتب شده است، بطوریکه بسیاری از خواص شیمیایی بصورت منظم در طول جدول تغییر نماید. جدول اولیه بدون اطلاع از ساختار داخلی اتمها ساخته شد: اگر عناصر را بر حسب جرم اتمی آنها مرتب نمائیم، و آنگاه نمودار خواص معین دیگر آنها را بر حسب جرم اتمی رسم نمائیم، میتوان نوسان یا تناوب این خواص را بصورت تابعی از جرم اتمی مشاهده نمود. اولین کسی که توانست این نظم را مشاهده نماید، یک شیمیدان آلمانی به نام Johann Wolfgang D?einer بود. او متوجه تعدادی تثلیث از عناصر مشابه شد:
|
نمونه تثلیث ها
|
||||||
| عنصر | جرم اتمی | چگالی | ------ | عنصر | جرم اتمی | چگالی |
| Cl | 35.5 | 1.56 g/L | ------ | Ca | 40.1 | 1.55 g/cm3 |
| Br | 79.9 | 3.12 g/L | ------ | Sr | 87.6 | 2.6 g/cm3 |
| I | 126.9 | 4.95 g/L | ------ | Ba | 137 | 3.5 g/cm3 |
و به دنبال او، شیمیدان انگلیسی John Alexander Reina Newlands متوجه گردید که عناصر از نوع مشابه در فاصلههای هشت تایی یافت می شوند، که آنها را با نتهای هشتگانه موسیقی شبیه نمود، هرچند که قانون نتهای او مورد تمسخر معاصرین او قرار گرفت. سرانجام شیمیدان آلمانی Lothar Meyer و شیمیدان روسی Dmitry Ivanovich Mendeleev تقریبا بطور همزمان اولین جدول تناوبی را، با مرتب نمودن عناصر بر حسب جرمشان، توسعه دادند( ولی مندلیف تعداد کمی از عناصر را خارج از ترتیب صریح جرمی، برای تطابق بهتر با خواص همسایگانشان رسم نمود – این کار بعدها با کشف ساختار الکترونی عناصر در اواخر قرن نوزدهم و اوایل قرن بیستم توجیه گردید). فهرست عناصر بر اساس نام، علامت اختصاری و عدد اتمی موجود میباشد. شکل زیر جدول تناوبی عناصر شناخته شده را نمایش میدهد. هر عنصر با عدد اتمی و علامتهای شیمیایی. عناصر در یک ستون ("گروه") از لحاظ شیمیایی مشابه می باشند.
| گروه | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | ||
| ردیف | ||||||||||||||||||||
| 1 | 1 H |
2 He |
||||||||||||||||||
| 2 | 3 Li |
4 Be |
5 B |
6 C |
7 N |
8 O |
9 F |
10 Ne |
||||||||||||
| 3 | 11 Na |
12 Mg |
13 Al |
14 Si |
15 P |
16 S |
17 Cl |
18 Ar |
||||||||||||
| 4 | 19 K |
20 Ca |
21 Sc |
22 Ti |
23 V |
24 Cr |
25 Mn |
26 Fe |
27 Co |
28 Ni |
29 Cu |
30 Zn |
31 Ga |
32 Ge |
33 As |
34 Se |
35 Br |
36 Kr |
||
| 5 | 37 Rb |
38 Sr |
39 Y |
40 Zr |
41 Nb |
42 Mo |
43 Tc |
44 Ru |
45 Rh |
46 Pd |
47 Ag |
48 Cd |
49 In |
50 Sn |
51 Sb |
52 Te |
53 I |
54 Xe |
||
| 6 | 55 Cs |
56 Ba |
* | 71 Lu |
72 Hf |
73 Ta |
74 W |
75 Re |
76 Os |
77 Ir |
78 Pt |
79 Au |
80 Hg |
81 Tl |
82 Pb |
83 Bi |
84 Po |
85 At |
86 Rn |
|
| 7 | 87 Fr |
88 Ra |
** | 103 Lr |
104 Rf |
105 Db |
106 Sg |
107 Bh |
108 Hs |
109 Mt |
110 Ds |
111 Uuu |
112 Uub |
113 Uut |
114 Uuq |
115 Uup |
116 Uuh |
117 Uus |
118 Uuo |
|
| * لانتانیدها | 57 La |
58 Ce |
59 Pr |
60 Nd |
61 Pm |
62 Sm |
63 Eu |
64 Gd |
65 Tb |
66 Dy |
67 Ho |
68 Er |
69 Tm |
70 Yb |
||||||
| ** آکتینیدها | 89 Ac |
90 Th |
91 Pa |
92 U |
93 Np |
94 Pu |
95 Am |
96 Cm |
97 Bk |
98 Cf |
99 Es |
100 Fm |
101 Md |
102 No |
||||||
| قلیائی فلزیها | قلیائی خاکیها | لانتانیدها | آکتینیدها | فلزات انتقالی |
| فلزات ضعیف | شبه فلزات | غیر فلزات | هالوژنها | گازهای کامل |
کد رنگ برای اعداد اتمی:
- عناصر شماره گذاری شده با رنگ آبی ، در دمای اتاق مایع هستند؛
- عناصر شماره گذاری شده با رنگ سبز ، در دمای اتاق بصورت گاز می باشند؛
- عناصر شماره گذاری شده با رنگ سیاه، در دمای اتاق جامد هستند.
- عناصر شماره گذاری شده با رنگ قرمز ترکیبی بوده و بطور طبیعی یافت نمی شوند(همه در دمای اتاق جامد هستند.)
- عناصر شماره گذاری شده با رنگ خاکستری ، هنوز کشف نشدهاند (و بصورت کم رنگ نشان داده شدهاند تا گروه شیمیایی را که در آن قرار می گیرند، مشخص نماید.(
و می توانید دراین کلید واژه جدول برای تشدید مغناطیسی را بیابید.
تعداد لایه الکترون در یک اتم تعیین کننده ردیفی است که در آن قرار می گیرد. هر لایه به زیرلایه های متفاوتی تقسیم میشود، که هر اندازه عدد اتمی افزایش می یابد، این لایه ها به ترتیب زیر:
1s
2s 2p
3s 3p
4s 3d 4p
5s 4d 5p
6s 4f 5d 6p
7s 5f 6d 7p
8s 5g 6f 7d 8p
...
به منظور بزرگنمايي جدول زير،روي آن راست كليك كرده وآن را ذخيره كنيد.جدول با اندازه بزرگ ذخيره خواهدشد.
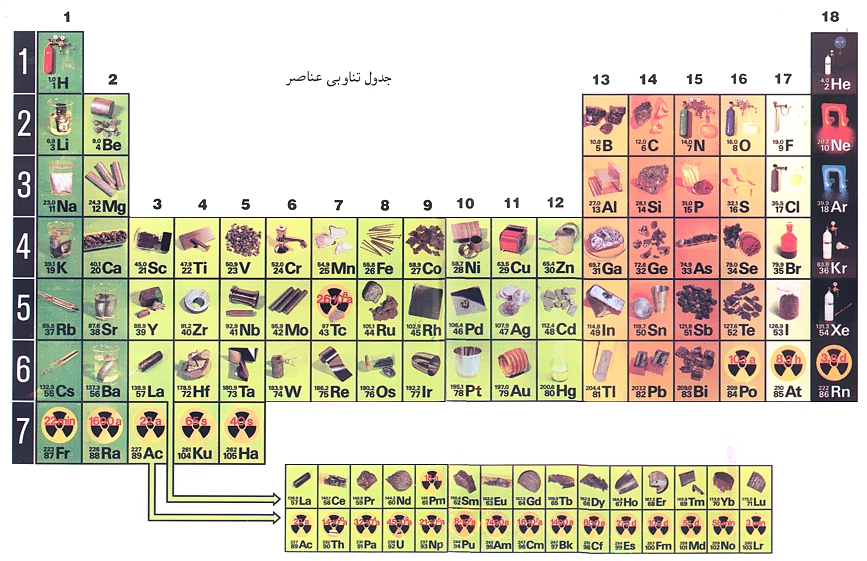
براساس ساختار جدول پر میشوند. از آنجائیکه الکترونهای خارجی ترین لایه، خواص شیمیایی را تعیین مینمایند، این لایه ها در میان گروهای یکسان مشابه اند.عناصر همجوار با یکدیگر در یک گروه، علیرغم اختلاف مهم در جرم، دارای خواص فیزیکی مشابه میباشند. عناصر همجوار با یکدیگر در یک ردیف دارای جرم های مشابه ولی خواص متفاوت میباشند.
برای مثال، عناصر بسیار نزدیک به نیتروژن (N) در ردیف دوم کربن(C) و اکسیژن(O) میباشند. علیرغم تشابه آنها در جرم ( که بصورت ناچیزی در واحد جرم اتمی تفاوت دارند)، دارای خواص بینهایت متفاوتی هستند، همانطور که با بررسی فرمهای دیگر میتوان ملاحظه نمود: اکسیژن دو اتمی یک کاز است که سوختن را تشدید می نماید، نیتروژن دو اتمی یک گاز است که سوختن را تشدید نمی کند، و کربن یک جامد است که میتواند سوزانده شود( بله، میتوان الماس را سوزاند!).
در مقایسه، عناصر بسیار نزدیک به کلر (Cl) در گروه یکی مانده به آخر در جدول «هالوژنها) فلوئور( F) و برم( Br) میباشند. علیرغم تفاوت فاحش جرم آنها در گروه، فرمهای دیگر آنها دارای خواص بسیار مشابه میباشند: آنها بسیار خورنده ( بدین معنی که تمایل خوبی برای ترکیب با فلزات، برای تشکیل نمک هالاید فلز)؛ کلر و فلوئور گاز هستند، درحالیکه برم یک مایع با تبخیر بسیار کم میباشد؛ کلر و برم بسیار رنگی هستند.
دانلود جدول تناوبي عناصر بافرمتPDF وكيفيت بي نهايت! با حجم 76 كيلوبايت
دانلود 6 پوستر باكيفيت وجالب جدول تناوبي با حجم 2.6 مگابايت
با سلام جهت استفاده از مطالب صلوات بر محمد و آل محمد بفرستيد و لطفاً لينك ما را در وبلاگ يا وبسايت خود قرار دهيد و به دوستان خود معرفي نماييد باتشكر - مديريت وبلاگ

نظرات شما عزیزان:
.: Weblog Themes By Pichak :.




 آمار
وب سایت:
آمار
وب سایت:

